Årsrapport fra Medicintilskudsnævnet 2009
Medlemmer udpeget af Indenrigs- og Sundhedsministeren 17 møder i 2009 21 ansøgninger om generelt tilskudBegrundelser 1632 ansøgninger om individuelle medicintilskudÅrlig vurdering af antallet af ansøgninger om enkelttilskud Møde i Medicintilskudsnævnets ekspertgruppeNordisk myndighedsmøde IRF’s efterårsmøde for regionale lægemiddelkonsulenterRevurdering af lægemidlers tilskudsstatus
Medicintilskudsnævnet rådgiver Lægemiddelstyrelsen i ansøgninger om tilskud til lægemidler. Det gælder både generelle tilskud til lægemidler (efter ansøgning fra lægemiddelvirksomheder) og individuelle tilskud til patienter (efter ansøgning fra læger). Nævnet rådgiver desuden Lægemiddelstyrelsen ved revurderinger af lægemidlers tilskudsstatus. Lægemiddelstyrelsen fungerer som sekretariat for nævnet.
Medlemmer udpeget af Indenrigs- og Sundhedsministeren
Medicintilskudsnævnet består af højst 7 medlemmer, hvoraf 2 skal være alment praktiserende læger. Medlemmerne udpeges af Indenrigs- og Sundhedsministeren efter indstilling fra Lægemiddelstyrelsen. Et medlem udnævnes efter indstilling fra Regionernes Lønnings- og Takstnævn. Nævnets medlemmer udpeges for 4 år ad gangen, og de har tilsammen en bred faglig ekspertise. Habilitetserklæringer for nævnets medlemmer kan ses på www.laegemiddelstyrelsen.dk.
I 2009 bestod nævnet af:
Overlæge, dr.med. Mogens Laue Friis (formand)
Overlæge, dr.med. Karine Bech
Alment praktiserende læge Ellen-Christine Beiter
Alment praktiserende læge Palle Mark Christensen fra 1. juli
Overlæge, dr.med. Thomas Gjørup fra 1. juli
Centerdirektør, dr.med. Mogens Sandbjerg Hansen til 1. juli
Alment praktiserende læge John Larsen
Udviklingschef Peder Ørnsholt Ring (Danske Regioner)
I juli 2009 startede en ny 4-årig periode for Medicintilskudsnævnet. Centerdirektør, dr.med. Mogens Sandbjerg Hansen stoppede i nævnet, og der kom to nye medlemmer ind i nævnet: alment praktiserende læge Palle Mark Christensen efter indstilling fra Dansk Selskab for Klinisk Farmakologi og overlæge, dr.med. Thomas Gjørup efter indstilling fra Dansk Selskab for Intern Medicin.
17 møder i 2009
Medicintilskudsnævnet holdt 17 møder i 2009, heraf 6 møder om revurdering af lægemidlers tilskudsstatus. Mødereferaterne kan læses på www.laegemiddelstyrelsen.dk.
21 ansøgninger om generelt tilskud
Medicintilskudsnævnet rådgiver Lægemiddelstyrelsen om ansøgninger om generelt tilskud efter de kriterier, som er fastsat i bekendtgørelse nr. 180 af 17. marts 2005 om medicintilskud.
I 2009 behandlede Medicintilskudsnævnet 21 ansøgninger om generelt tilskud. Flere af ansøgningerne blev behandlet på mere end 1 møde. 9 lægemidler blev indstillet til generelt tilskud uden klausulering, 2 lægemidler blev indstillet til generelt tilskud med klausulering, heraf blev det klausulerede tilskud for 1 lægemiddel indstillet til at blive udvidet. 10 lægemidler blev indstillet til afslag, heraf blev tilskudsstatus for et lægemiddel ændret fra generelt tilskud uden klausulering til generelt tilskud med klausulering. 4 af ansøgningerne var genansøgninger. 2 ansøgninger blev udsat til et af de efterfølgende møder, fordi nævnet i det ene tilfælde havde behov for en faglig udtalelse fra et videnskabeligt selskab inden endelig stillingtagen til den aktuelle ansøgning. I det andet tilfælde ønskede nævnet at få vurderet et firmas sundhedsøkonomiske analyse af Dansk Sundhedsinstitut (DSI). Antallet af ansøgninger om generelt tilskud, som nævnet behandlede på de månedlige møder, fremgår af figur 1.
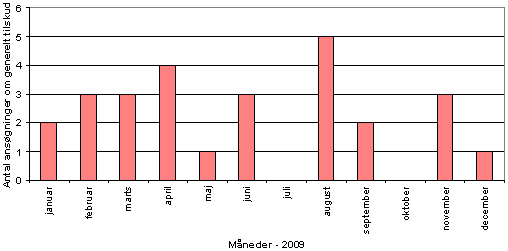
Figur 1. Antal ansøgninger om generelt tilskud behandlet af nævnet pr. månedligt møde i 2009.
Begrundelser
Nævnets indstillinger i forbindelse med ansøgninger om generelt tilskud offentliggøres på Lægemiddelstyrelsens hjemmeside. Indstillingerne til afslag har bl.a. været begrundet i lægemidlernes pris sammenlignet med andre relevante lægemidler, og i risikoen for anvendelse af lægemidlerne som førstevalg, uanset at dette efter nævnets opfattelse ikke bør være tilfældet.
Indstillingerne til generelt tilskud har oftest været begrundet i, at den behandlingsmæssige værdi står mål med prisen sammenlignet med andre relevante lægemidler.
1632 ansøgninger om individuelle medicintilskud
I 2009 afgjorde Lægemiddelstyrelsen 138.715 ansøgninger om individuelle medicintilskud. 1632 af disse ansøgninger blev forelagt for Medicintilskudsnævnet, fordi sekretariatet ikke umiddelbart mente, de kunne imødekommes. I 31 pct. af tilfældene indstillede nævnet, at ansøgningerne skulle imødekommes. Antallet af individuelle ansøgninger, som nævnet behandlede på de månedlige møder, fremgår af figur 2.
I forbindelse med behandling af ansøgninger om enkelttilskud drøfter nævnet jævnligt, om de vejledende kriterier for enkelttilskud til de forskellige lægemidler er i overensstemmelse med nyeste viden indenfor de pågældende sygdomsområder. I løbet af året blev de vejledende enkelttilskudskriterier for lægemidler mod neuropatiske smerter, græspollenallergi og refraktær svær kronisk håndeksem således opdateret.
Årlig vurdering af antallet af ansøgninger om enkelttilskud
Lægemiddelstyrelsen udarbejder hvert år en status over antal ansøgninger om enkelttilskud i året, der er gået. På baggrund af denne status diskuterer nævnet fordelingen mellem imødekomne og afslåede ansøgninger inden for de respektive lægemidler/lægemiddelgrupper, herunder om udviklingen i antallet af ansøgninger er hensigtsmæssig. Nævnet indstillede på dette grundlag ingen lægemidler/lægemiddelgrupper til generelt eller generelt klausuleret tilskud i 2009.
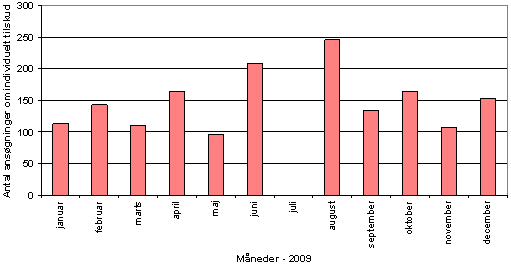
Figur 2. Antallet af individuelle tilskudsansøgninger behandlet af nævnet pr. månedligt møde i 2009.
Møde i Medicintilskudsnævnets ekspertgruppe
Den 12. maj holdt Medicintilskudsnævnets ekspertgruppe nedsat til drøftelse af spørgsmålet om medicintilskud til alitretinoin møde. Ekspertgruppen består af repræsentanter fra Dansk Dermatologisk Selskab og to medlemmer fra nævnet – formanden Mogens Laue Friis og Ellen-Christine Beiter. Lægemiddelstyrelsen varetog sekretariatsfunktionen.
Ekspertgruppen blev indkaldt med henblik på diskussion og eventuel revurdering af de gældende vejledende kriterier for enkelttilskud til alitretinoin til behandling af patienter med refraktær kronisk svær håndeksem.
Nordisk myndighedsmøde
Mogens Laue Friis deltog i et nordisk myndighedsmøde, som blev afholdt i Oslo den 10.-11. september. Formålet med mødet var primært at drøfte emner af særlig interesse for pris- og tilskudsmyndighederne herunder en orientering fra de enkelte lande om, hvad der var sket på dette område siden sidste nordiske myndighedsmøde. Sverige præsenterede en stor omregulering af apotekerne, herunder ophør af apoteksmonopolet. Finland præsenterede et nyt referenceprissystem, samt forslag til ordinationsret for sygeplejersker. Island præsenterede forskellige tiltag for at sænke lægemiddeludgifterne. Norge præsenterede en ny prisundersøgelse, erfaringer med en ny indikationsbaseret refusionsliste og forbedringer af enkelttilskudsordningen inspireret af et studiebesøg i Danmark. Fra dansk side blev orienteret om den nyligt ændrede tilskudsstatus for blodtrykslægemidlerne, rapporten om sygehuslægemidler og prisloftaftalen. Endelig blev en række nye lægemidler gennemgået med henblik på tilskudsstatus i de enkelte lande.
IRF’s efterårsmøde for regionale lægemiddelkonsulenter
Den 6. oktober holdt Mogens Laue Friis et oplæg om medicintilskud til farmakologisk behandling af ADHD på IRF’s efterårsmøde for de regionale lægemiddelkonsulenter. IRF afholder hvert år et møde for de regionale lægemiddelkonsulenter for at skabe grundlag for en uformel udveksling af erfaringer og synspunkter med det formål at medvirke til en optimering af de regionale lægemiddelkonsulenters indsats.
Revurdering af lægemidlers tilskudsstatus
Lægemiddelstyrelsen skal ifølge sundhedsloven løbende revurdere alle lægemidlers tilskudsstatus. Medicintilskudsnævnet udarbejder indstillinger med anbefaling om lægemidlers fremtidige tilskudsstatus til Lægemiddelstyrelsen. De overordnede kriterier for prioritering af revurderingen af de enkelte lægemiddelgrupper er lægemidlernes betydning for primærsektoren og specielt almen praksis, folkesundhedsmæssige aspekter, eventuelle nye evidensbaserede anbefalinger, store udgifter for patient og region samt et stort forbrug. Med udgangspunkt heri anbefalede Medicintilskudsnævnet i 2009, at Lægemiddelstyrelsen i 2010 begynder revurdering af tilskudsstatus for lægemidler i følgende grupper i nævnte rækkefølge: antibakterielle midler til systemisk brug, antidepressiva, opioider og antidiabetika.
I 2009 har nævnet drøftet tilskudsstatus for følgende lægemiddelgrupper:
- Laksantia
- Midler mod fedme ekskl. diætmidler
- Antiemetika og midler mod kvalme
- Peristaltikfremmende midler
- Perifere vasodilatorer
- Vasoprotektiva
- Midler mod syrerelaterede forstyrrelser
foruden at nævnet løbende har fulgt blodtrykslægemidlerne, og herunder forbrugsændringerne, før og efter tilskudsændringen den 13. juli 2009.
Af ovenstående lægemiddelgrupper blev nævnets indstillinger for fedmemidler ekskl. diætmidler, laksantia og magnesiumhydroxid, antiemetika og midler mod kvalme, peristaltikfremmende midler, perifere vasodilatorer, vasoprotektiva og midler mod syrerelaterede forstyrrelser sendt i høring hos berørte virksomheder, relevante organisationer og relevante videnskabelige selskaber. Høringssvarene kan læses på www.laegemiddelstyrelsen.dk.
Høringsfristen på midler mod syrerelaterede forstyrrelser udløb den 15. marts 2010. I kun en enkelt af de øvrige grupper var der indkommet høringssvar. Disse blev drøftet af nævnet, som ikke fandt anledning til at ændre sin indstilling. Lægemiddelstyrelsen fulgte nævnets indstillinger og har truffet afgørelse indenfor følgende grupper: laksantia, midler mod fedme ekskl. diætmidler, antiemetika og midler mod kvalme, peristaltikfremmende midler og perifere vasodilatorer. Tilskudsstatus for metoclopramid (A03FA01) tabletter og hårde depotkapsler og domperidon (A03FA03) tabletter blev ændret, således at disse lægemidler fik generelt tilskud den 14. december 2009. De øvrige lægemidlers tilskudsstatus forblev uændret. Lægemiddelstyrelsens afgørelser kan læses på www.laegemiddelstyrelsen.dk.
Medicintilskudsnævnet
