Eylea 40 mg/ml (aflibercept injektionsvæske til intravitreal injektion): Øget risiko for forhøjet intraokulært tryk med den forfyldte injektionssprøjte
Eylea 40 mg/ml (aflibercept injektionsvæske til intravitreal injektion): Øget risiko for forhøjet intraokulært tryk med den forfyldte injektionssprøjte
Bayer vil efter aftale med Det Europæiske Lægemiddelagentur og Lægemiddelstyrelsen gerne informere om følgende.
Resumé
- Tilfælde af forhøjet intraokulært tryk er blevet rapporteret hyppigere (estimeret op til 7 gange hyppigere) når den forfyldte injektionssprøjte med Eylea anvendes, sammenlignet med administration af Eylea i hætteglas hvor en Luer-lock-sprøjte anvendes.
- Det mistænkes, at fejlhåndtering i forberedelsen og injektionen er den mest sandsynlige årsag til de observerede tilfælde af forhøjet intraokulært tryk med den forfyldte injektionssprøjte med Eylea. Injektionerne skal administreres af en sundhedsperson, der har erfaring med håndtering af denne formulering.
- Korrekt håndtering af den fyldte injektionssprøjte og træning er afgørende for at reducere denne risiko:o brug en 30 G x ½" injektionskanyle;
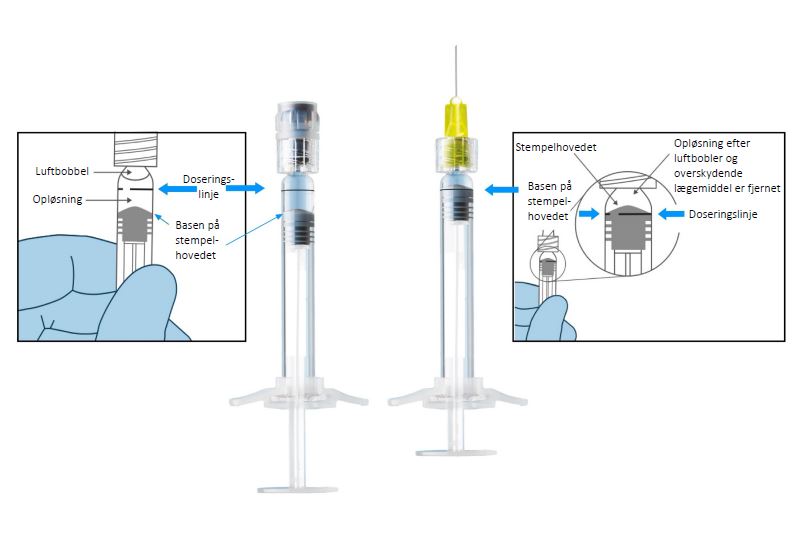
- kontrollér altid at overskydende væske/luftbobler i den forfyldte injektionssprøjte er fjernet før anvendelse: basen på stempelhovedet (ikke spidsen af stempelhovedet) skal være på linje med den sorte doseringslinje på injektionssprøjten (se nedenfor); o tryk stemplet forsigtigt ned;
- administrér den præcise anbefalede dosis og injicer ikke eventuel resterende volumen, da en øget injektionsvolumen kan føre til klinisk relevant forhøjet intraokulært tryk.
- Evaluér patientens syn og overvåg det intraokulære tryk umiddelbart efter den intravitreale injektion.
Baggrundsinformation
Eylea forfyldt injektionssprøjte er indiceret til voksne til behandling af:
- neovaskulær (våd) aldersrelateret makulær degeneration (AMD),
- nedsat syn på grund af makulaødem sekundært til retinal veneokklusion (RVO)
(grenveneokklusion eller centralveneokklusion),
- nedsat syn på grund af diabetisk makulaødem (DME),
- nedsat syn på grund af myopisk koroidal neovaskularisering (myopisk CNV).
Forhøjet intraokulært tryk er en kendt bivirkning associeret med intravitreale injektioner generelt, herunder injektioner med Eylea. Der er 7 gange flere indberetninger af tilfælde med forhøjet intraokulært tryk med den forfyldte injektionssprøjte (ca. 1,1 tilfælde per 10.000 solgte forfyldte injektionssprøjter versus 0,15 tilfælde per 10.000 solgte hætteglas) efter den europæiske lancering af produktet i april 2020. Der har været indberetninger af forbigående stigninger i det intraokulære tryk og reversibel nedsat syn efter intravitreale injektioner.
Blandt tilfældene med kendt udfald gik størstedelen over uden varige følgestilstande.
Der er ikke detekteret nogen fejl i kvaliteten af den forfyldte injektionssprøjte med Eylea eller opløsningen, som skal injiceres. Efter yderligere gennemgang af de indberettede tilfælde mistænkes det, at årsagen til forhøjet intraokulært tryk kan være administrering af overskydende lægemiddel på grund af fejlhåndtering i forberedelsen og injektionen . Ydermere, er den fyldte injektionssprøjte med Eylea en glassprøjte med et stempel af gummi, som kræver en anelse flere kræfter at bruge, sammenlignet med plastiksprøjten (som anvendes ved administrationsmetoden med hætteglas). For at minimere denne risiko, skal følgende anbefalinger vedrørende hensigtsmæssig håndtering af den forfyldte injektionssprøjte med Eylea, følges nøje:
- En 30 gauge x ½" injektionskanyle skal anvendes.
- For at fjerne bobler og sprøjte overskydende lægemiddel ud, skal stemplet placeres korrekt. Basen på stempelhovedet (ikke spidsen af stempelhovedet) skal være på linje med den sorte doseringslinje på injektionssprøjten, som beskrevet i afsnittet ”Brugsanvisning til fyldt injektionssprøjte” i produktinformationen og i figuren nedenfor.
- Når dosen administreres i øjet, skal stemplet forsigtigt trykkes ned med konstant tryk indtil stemplet når bunden af injektionssprøjten. Et lille residualvolumen af opløsningen kan ses i injektionssprøjten efter stemplet har nået bunden af injektionssprøjten. Forsøg ikke at injicere dette ved at trykke yderligere ned på stemplet.
- Passende overvågning af det intraokulære tryk kan bestå af kontrol af perfusion af det optiske nervehoved eller tonometri. Sterilt udstyr til paracentese bør være disponibelt.
Det anbefales at se det udleverede træningsmateriale og den udleverede information vedrørende korrekt brug af den forfyldte injektionssprøjte som er beskrevet i vejledningen til den ordinerende læge og i videoen om injektionsprocedure, som indgår i uddannelsesmaterialet for Eylea. Uddannelsesmaterialet, herunder patientvejledning, er også tilgængelig på www.edumaterial.bayer.dk eller kan udleveres efter anmodning sammen med træningssessioner.
Produktinformationen og uddannelsesmaterialet til sundhedspersoner opdateres så de indeholder yderligere vejledninger/anbefalinger vedrørende håndteringen af den forfyldte injektionssprøjte for at reducere risikoen for forhøjet intraokulært tryk.
Indberetning af formodede bivirkninger
Indberetning af formodede bivirkninger er vigtig. Dette muliggør løbende overvågning af benefit/risk-forholdet for lægemidlet. Sundhedspersoner anmodes om at indberette alle formodede bivirkninger forbundet med brugen af Eylea via:
Lægemiddelstyrelsen
Axel Heides Gade 1
DK-2300 København S
Websted: www.meldenbivirkning.dk
Virksomhedens kontaktoplysninger
Hvis du har spørgsmål eller brug for yderligere information vedrørende korrekt brug af den forfyldte injektionssprøjte med Eylea, kontakt venligst afdeling for medicinsk information hos Bayer A/S på:
Telefon: 45 23 50 00
