Årsrapport fra Medicintilskudsnævnet 2006
Medlemmer udpeget af indenrigs- og sundhedsministeren
19 møder i 2006
20 ansøgninger om generelt tilskud
1850 ansøgninger om individuelle medicintilskud
Høring på Christiansborg om substitution af epilepsimedicin
Nordisk myndighedsmøde
Retssag mod Indenrigs- og Sundhedsministeriet og Lægemiddelstyrelsen
Uautoriserede ansøgningsskemaer
Revurdering af lægemidlernes tilskudsstatus
I denne rapport kan du læse om Medicintilskudsnævnets arbejde i 2006.
Medicintilskudsnævnet rådgiver Lægemiddelstyrelsen i sager om medicintilskud til lægemidler - såvel generelle tilskud til lægemidler (efter ansøgning fra lægemiddelvirksomheder) som individuelle tilskud til patienter (efter ansøgning fra læger). Nævnet rådgiver desuden Lægemiddelstyrelsen ved revurderinger af lægemidlers tilskudsstatus. Lægemiddelstyrelsen fungerer som sekretariat for nævnet.
Medlemmer udpeget af indenrigs- og sundhedsministeren
Medicintilskudsnævnet har 6 medlemmer, der er udpeget af indenrigs- og sundhedsministeren efter indstilling fra Lægemiddelstyrelsen og de videnskabelige selskaber. Et medlem udnævnes dog efter indstilling fra Regionernes Lønnings- og Takstnævn. Nævnets medlemmer udpeges for 4 år ad gangen, og de har tilsammen en bred faglig ekspertise. Habilitetserklæringer for nævnets medlemmer kan ses fra faktaboksen til højre.
I 2006 bestod nævnet af:
Overlæge, dr. med. Mogens Laue Friis (formand)
Overlæge, dr.med. Karine Bech
Alment praktiserende læge Ellen- Christine Beiter
Centerdirektør, dr.med. Mogens Sandbjerg Hansen
Kontorchef Lilly Krogsgaard (Amtsrådsforeningen)
Alment praktiserende læge John Larsen.
19 møder i 2006
I 2006 holdt Medicintilskudsnævnet 19 møder. Mødereferaterne kan læses fra faktaboksen til højre.
20 ansøgninger om generelt tilskud
Medicintilskudsnævnet rådgiver Lægemiddelstyrelsen om ansøgninger om generelt tilskud efter de kriterier, som er fastsat i Bekendtgørelse nr. 180 af 17. marts 2005 om medicintilskud.
I 2006 behandlede Medicintilskudsnævnet 20 ansøgninger om generelt tilskud. 12 lægemidler blev indstillet til generelt tilskud, 8 til afslag. 3 af ansøgningerne var genansøgninger. 2 af disse lægemidler blev indstillet til generelt tilskud. Antallet af ansøgninger om generelt tilskud, som nævnet behandlede på de månedlige møder, fremgår af figur 1. I tabel 1 ses en gengivelse af begrundelserne for nævnets indstillinger til afslag.
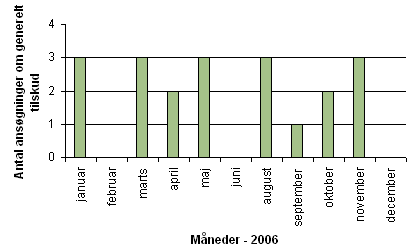
Figur 1. Antal ansøgninger om generelt tilskud behandlet af nævnet pr. månedligt møde i 2006.
Begrundelser for afslag |
Antal ansøgninger |
Der er risiko for, at lægemidlet vil blive anvendt udenfor den godkendte indikation, og der er risiko for, at lægemidlet vil blive anvendt som førstevalg. |
2 |
Lægemidlets pris står ikke i rimeligt forhold til lægemidlets behandlingsmæssige værdi. |
1 |
Der er risiko for, at lægemidlet vil blive anvendt som førstevalg. |
1 |
Der er risiko for, at lægemidlet vil blive anvendt uden for den godkendte indikation. |
1 |
Iværksættelse af behandling med lægemidlet kræver særlig undersøgelse og diagnosticering. |
1 |
Lægemidlets pris står ikke i rimeligt forhold til lægemidlets behandlingsmæssige værdi, og der er risiko for, at lægemidlet vil blive anvendt som førstevalg. |
1 |
Lægemidlets pris står ikke i rimeligt forhold til lægemidlets behandlingsmæssige værdi, og der er risiko for, at lægemidlet vil blive anvendt uden for den godkendte indikation. |
1 |
Tabel 1. Afslagsbegrundelser for ansøgninger om generelt tilskud i 2006.
1850 ansøgninger om individuelle medicintilskud
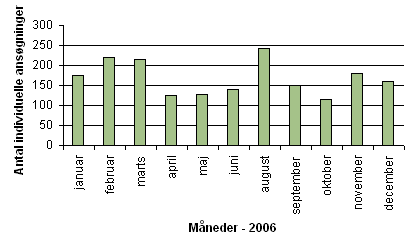
I 2006 behandlede nævnet 1850 ansøgninger om individuelle medicintilskud, som sekretariatet ikke umiddelbart mente kunne imødekommes. I 46 pct. af tilfælde indstillede nævnet, at ansøgningerne skulle imødekommes. Antallet af individuelle ansøgninger, som nævnet behandlede på de månedlige møder, fremgår af figur 2.
Figur 2. Antallet af individuelle tilskudsansøgninger behandlet af nævnet pr. månedligt møde i 2006.
Høring på Christiansborg om substitution af epilepsimedicin
Mogens Laue Friis, der er formand for Medicintilskudsnævnet, deltog som oplægsholder og paneldeltager på en høring, der var arrangeret af Dansk Epilepsiforening på Christiansborg den 21. marts 2006. Mogens Laue Friis holdt et oplæg om Medicintilskudsnævnets lægefaglige rådgivning af Lægemiddelstyrelsen ved ansøgninger om forhøjet tilskud til lægemidler mod epilepsi og deltog i den efterfølgende debat.
Nordisk myndighedsmøde
Mogens Laue Friis deltog i et nordisk myndighedsmøde om landenes erfaring med primært myndighedernes administration af lægemiddelpriser og medicintilskud. Mødet blev holdt den 19. til 20. juni 2006 i Stockholm. Foruden en orientering fra de enkelte lande om, hvad der var sket på dette område siden sidste nordiske myndighedsmøde, var der fokus på Sveriges og Danmarks erfaringer med revurdering af lægemidlers tilskudsstatus. Deltagerne diskuterede også mulighederne for et fremtidigt større samarbejde på dette område.
Retssag mod Indenrigs- og Sundhedsministeriet og Lægemiddelstyrelsen
Lægemiddelvirksomheden Merck Sharp & Dohme (MSD) anlagde i 2003 retssag mod Indenrigs- og Sundhedsministeriet og Lægemiddelstyrelsen, der havde afslået en ansøgning om generelt tilskud til MSD’s lægemiddel Fosamax®. Mogens Laue Friis og Karen Kolenda (sektionsleder i Lægemiddelstyrelsen) afgav vidneforklaring i Østre Landsret den 25. september 2006. Landsretten afsagde dom den 19. december 2006. Indenrigs- og Sundhedsministeriet og Lægemiddelstyrelsen blev frifundet.
Østre Landsret anerkendte i dommen, at Medicintilskudsnævnets og Lægemiddelstyrelsen har ret til at udøve et fagligt begrundet skøn, fordi nævnet og Lægemiddelstyrelsen har en særlig erfaring og faglig indsigt på området. Ligeledes tilsluttede Østre Landsret sig Lægemiddelstyrelsens forståelse af udtrykket ”behandling” i den godkendte indikation for Fosamax®. Lægemiddelstyrelsen har tillagt udtrykket selvstændig betydning, så indikationen skal forstås i overensstemmelse med de kriterier, der gælder for behandlingskrævende osteoporose. Endvidere fandt Østre Landsret, at afslaget ikke var i strid med proportionalitetsprincippet, og at der ikke var blevet varetaget usaglige hensyn i afgørelsen.
Uautoriserede ansøgningsskemaer
Nævnet oplevede i 2006 flere eksempler på betydelig kreativitet: Produktspecialister fra lægemiddelindustrien gav forkerte oplysninger til læger om ansøgning om enkelttilskud, og uautoriserede skemaer til ansøgning om individuelle tilskud på bestemte virksomheders lægemidler blev udleveret til lægerne. Skemaerne fremtrådte, som om de var udarbejdet af Lægemiddelstyrelsen. Nævnet blev også præsenteret for en mappe udarbejdet af en lægemiddelvirksomhed med forslag til, hvordan lægerne skulle søge om enkelttilskud på en række af virksomhedens produkter (for at opnå tilskud). Mappen indeholdt også forslag til en standardklagevejledning, hvis en ansøgning ikke skulle blive imødekommet.
Revurdering af lægemidlernes tilskudsstatus
Lægemiddelstyrelsen skal ifølge sundhedsloven revurdere alle lægemidlers tilskudsstatus over perioder på 5 år. Projektet startede i sommeren 2005 efter anbefaling af Indenrigs- og Sundhedsministeriets udvalg om medicintilskud, jf. betænkning nr.1444 fra maj 2004 om Medicintilskud og rigtig anvendelse af lægemidler. Alle lægemidler bliver gennemgået for at sikre, dels at de lægemidler, som har generelt tilskud, stadig opfylder de kriterier, der gælder, og dels at der ikke er lægemidler uden generelt tilskud, som opfylder kriterierne. Medicintilskudsnævnet udarbejder indstillinger til Lægemiddelstyrelsen om tilskudsstatus.
I 2006 har nævnet drøftet tilskudsstatus for følgende lægemiddelgrupper:
- Lipidsænkende lægemidler
- Lægemidler til behandling af hypertension
- Lægemidler til hjerteterapi
- Perifere kardilaterende midler
- Midler mod åreknuder og hæmorider.
Nævnets indstilling for lægemiddelgruppen lipidsænkende lægemidler blev i efteråret 2006 sendt i høring hos berørte virksomheder og relevante videnskabelige selskaber.
Yderligere oplysninger kan fås ved henvendelse til Lægemiddelstyrelsens sekretariat for Medicintilskudsnævnet på Send en mail.