Undersøgelser af AstraZeneca-vaccinen
I dette tema kan du læse om lægemiddelmyndighedernes undersøgelse af det sjældne og usædvanlige sygdomsbillede med lavt blodpladetal, blodpropper og blødning efter vaccinationer med AstraZenecas vaccine mod COVID-19 (Vaxzevria).
TemaAstraZeneca-vaccinen Vaxzevria er en af de indtil videre fire vacciner mod COVID-19, som er godkendt af det europæiske lægemiddelagentur EMA.
Den 11. marts gik EMA i gang med at lavet en vurdering af de sjældne, men alvorlige bivirkninger, der er set efter vaccination med COVID-19 vaccinen fra AstraZeneca. Samtidig er der gennemført en række undersøgelser i Danmark.
Vaxzevria er sandsynligvis årsag til sjældent, alvorligt sygdomsbillede med blodpropper kombineret med et lavt antal blodplader og blødning. Det har en ekspertgruppe nedsat af EMA konkluderet.
Konklusionen ændrer dog ikke på, at AstraZenecas COVID-19-vaccine fortsat er godkendt af lægemiddelmyndighederne, fordi fordelene ift. at modvirke dødsfald og andre sundhedsmæssige konsekvenser af COVID-19 stadig opvejer de mulige risici i form af kendte og mulige bivirkninger.
Status i Danmark
Lægemiddelstyrelsen har modtaget to danske indberetninger, hvor det er konstateret, at der er tale om det særlige sygdomsbillede, efter vaccination med Vaxzevria.
Både de to danske tilfælde og de lignende tilfælde, der er indberettet i andre lande, er hovedsageligt opstået inden for de første 14 dage efter vaccinationen. Det ene tilfælde i Danmark har haft dødeligt udfald.
På baggrund af sammenhængen mellem AstraZeneca-vaccinen og disse tilfælde af det sjældne sygdomsbillede og sammenholdt med, at der generelt er en god kontrol med COVID-19 epidemien i Danmark, og at der er andre tilgængelige vacciner mod COVID-19, har Sundhedsstyrelsen besluttet at fortsætte vaccinationen mod COVID-19 uden vaccinen fra AstraZeneca.
Link til Sundhedsstyrelsens nyhed: Danmark fortsætter vaccineudrulning uden AstraZeneca-vaccinen
Nyheder fra Lægemiddelstyrelsen
Spørgsmål og svar om AstraZeneca-vaccinen (Vaxzevria)
Hvad skal jeg gøre, hvis jeg har fået en vaccination med Vaxzevria?
Det er vigtigt at bemærke, at de indberettede tilfælde af blodpropper kombineret med et lavt antal blodplader er meget sjældne, og at vaccinerne modvirker COVID-19 og generelt giver et lettere sygdomsforløb, hvis man får symptomer, selvom man er vaccineret. Man bør derfor ikke være bekymret, hvis man har modtaget vaccinen, men blot opmærksom inden for 14 dage efter vaccinationen. Læs Lægemiddelstyrelsens brev den 15. marts til borgere vaccineret med AstraZeneca.
Hvilke bivirkninger er almindelige efter Vaxzevria?
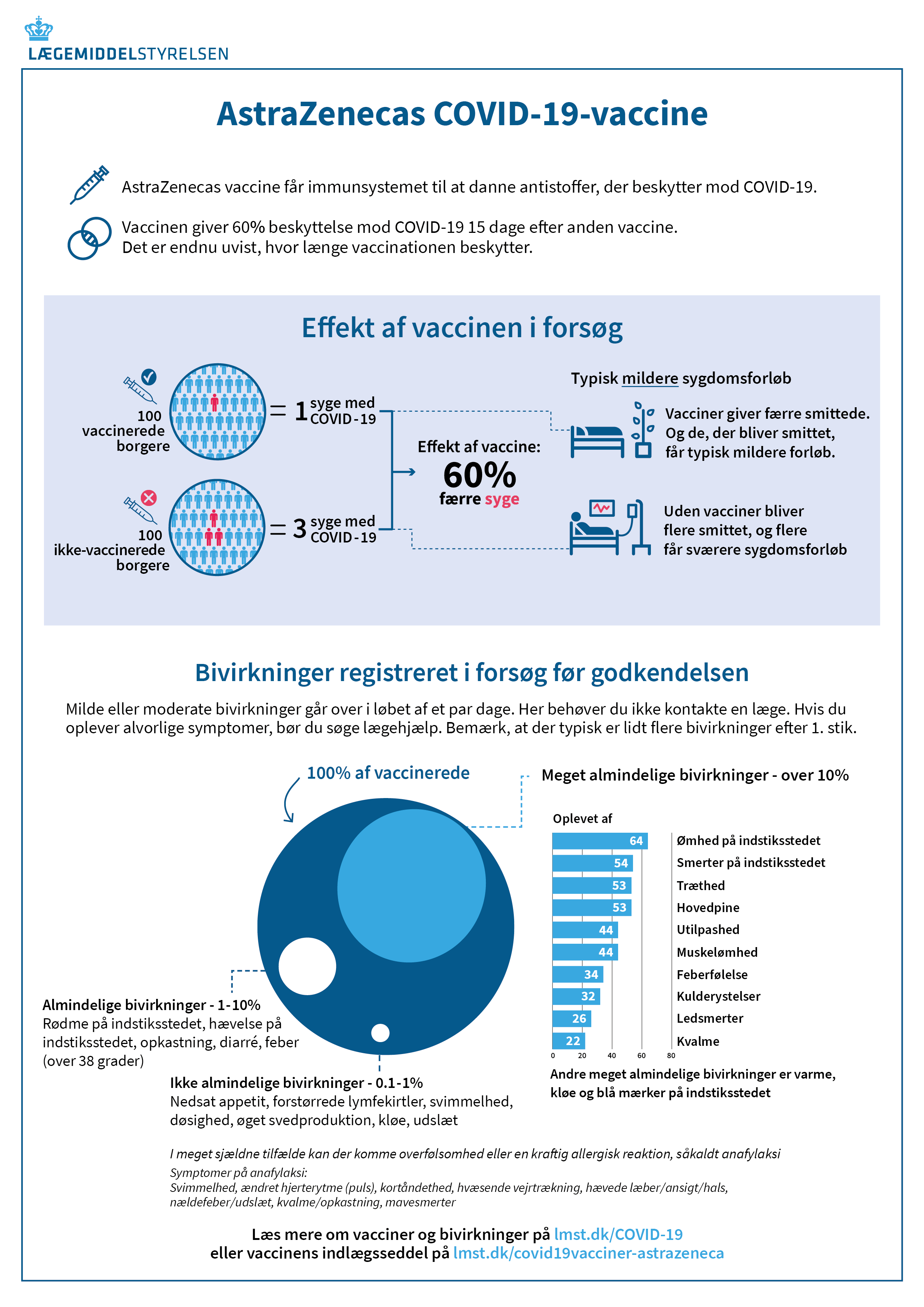
De almindelige symptomer er lette til moderate, forbigående bivirkninger som smerter og rødme ved indstiksstedet, træthed, hovedpine, muskel- og ledsmerter, kulderystelser og feber. Når en vaccine aktiverer immunsystemet, vil mange opleve influenzalignende symptomer. Det er helt almindeligt og et tegn på, at kroppens immunsystem reagerer på vaccinen og booster kroppens forsvarsværk mod COVID-19.
Hvad er symptomerne på et lavt antal blodplader og blodpropper?
Et blåt mærke på indstiksstedet er forventeligt, men et lavt antal blodplader kan påvirke blodets evne til at størkne. Symptomer på et lavt antal blodplader kan være en større tendens til at få blå mærker, små punktformede blødninger i huden eller blødninger, der ikke stopper, som de plejer.
Der kan være forskellige symptomer på blodpropper afhængigt af, hvor i kroppen de opstår. Symptomer kan f.eks. være kraftig hovedpine, kraftige mavesmerter, at benet bliver koldt, pludselige og uventede smerter i dele af kroppen vejrtrækningsbesvær eller lammelser i den ene side af kroppen.
Hvor alvorlige er de mistænkte tilfælde af bivirkninger?
De kan være alvorlige, og både i Danmark og EU har der været dødsfald. Det undersøges i øjeblikket, om der er en årsagsforbindelse mellem vaccinationen og symptomerne.
Lægemiddelstyrelsens informationsark om AstraZeneca-vaccinen
Links
Link til Sundhedsstyrelsens nyhed: Danmark fortsætter vaccineudrulning uden AstraZeneca-vaccinen
Links til nyheder fra det europæiske lægemiddelagentur EMA om AstraZeneca-vaccinen (Vaxzevria):
AstraZeneca’s COVID-19 vaccine: EMA finds possible link to very rare cases of unusual blood clots with low blood platelets
(07.04.2021 - på engelsk)
COVID-19 Vaccine AstraZeneca – Update on ongoing evaluation of blood clot cases
(25.03.2021 - på engelsk)
COVID-19 Vaccine AstraZeneca: benefits still outweigh the risks despite possible link to rare blood clots with low blood platelets
(18.03.2021 - på engelsk)
Investigation of COVID-19 Vaccine AstraZeneca and thromboembolic events continues
(16.03.2021 - på engelsk)
EMA’s safety committee continues investigation of COVID-19 Vaccine AstraZeneca and thromboembolic events – further update
(15.03.2021 - på engelsk)
COVID-19 Vaccine AstraZeneca: PRAC investigating cases of thromboembolic events - vaccine’s benefits currently still outweigh risks - Update
(11.03.2021 - på engelsk)
Generelt om AstraZeneca-vaccinen (Vaxzevria)
Hvordan virker Vaxzevria?
På vores tema om godkendte vacciner kan du læse om:
- Hvordan vaccinen Vaxzevria virker
- Hvilken effekt vaccinen har
- Grundlaget for den betingede godkendelse
- De mest almindelige bivirkninger
- Indlægsseddel og produktresume
Link til informationer om effekt, indlægsseddel og bivirkninger ved AstraZeneca vaccinen (Vaxzevria)
Indberettede bivirkninger ved Vaxzevria
Under vores tema om indberettede bivirkninger kan du læse:
- Antal personer der har påbegyndt vaccination med Vaxzevria
- Antal færdigvaccinerede personer
- Antal indberetninger om formodede bivirkninger
- Antal behandlede indberetninger om formodede bivirkninger
- Hvilke bivirkninger, der er indberettet og fordelingen på alder
Link til indberettede, formodede bivirkninger om AstraZeneca vaccinen (Vaxzevria)
Overvågning af bivirkninger
Lægemiddelstyrelsen registrerer, overvåger og vurderer indberetninger om formodede bivirkninger i Danmark. Nye vacciner og ny medicin bliver overvåget nøje. Det gælder også for COVID-19-vaccinerne, herunder AstraZeneca vaccinen (Vaxzevria).
Lægemiddelstyrelsen samarbejder med bl.a. lægemiddelmyndighederne i EU, det europæiske medicinalagentur EMA og verdenssundhedsorganisationen WHO om overvågning af sikkerheden ved COVID-19-vaccinerne.
Læs mere om det store arbejde med at overvåge bivirkningerne ved vaccinen